
Adiabatický děj
Soustava, ve které probíhá adiabatický děj, je tepelně izolovaná od okolí. V praxi to znamená, že nedochází ke sdílení tepla ze soustavy na okolí a naopak. Stavové veličiny teplota T, tlak p a objem V na rozdíl od předcházejících tří případů nejsou konstantní.
Plyn koná práci na úkor své vnitřní energie, takže W = - D U. Vyplývá to z prvního termodynamického principu. Pro jeden mol ideálního plynu při adiabatickém ději platí Poissonův zákon:![]() =
konst.
=
konst.
g ve vztahu je poměr měrných tepelných kapacit. Dříve byl používán název Poissonova konstanta. Poměr měrných tepelných kapacit je definován vztahem
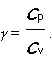
![]()
![]()
V technické
praxi probíhají děje blížící se adiabatickým velmi rychle. Minimalizuj se tak sdílení tepla s okolím . Část tepla ale pochopitelně ztratíme při sdílení tepla s okolím vždy. Při rychlé expanzi plynu se může ochladit na velmi nízké teploty. Na změně vnějšího tlaku je založen princip sněhových hasicích přístrojů. Za adiabatický děj v praxi považujeme nafukování kola pumpičkou, samozapálení směsi u vznětového motoru i šíření zvuku.





