
Molekulový tlak, též soudržnostní tlak, též kohezní tlak je tlak působící uvnitř kapaliny. Molekuly uvnitř kapaliny na sebe působí přitažlivými silami. Je však důležité,
kde se popisovaná molekula nachází. Výslednice přitažlivých sil působících na molekulu kapaliny je různá proAd 1. Pokud je molekula uvnitř kapaliny,
tak silové působení sousedních molekul kapaliny je rovnoměrně rozloženo do všech směrů. Výslednice všech sil je pak prakticky rovna nule. Přitažlivé síly mezi molekulami jsou krátkodosahové. Jejich velikost značně klesá se vzdáleností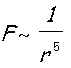
V praxi je tato vzdálenost asi r0 = 10-9 m. Všechny molekuly vzdálené od sledované částice maximálně o r0
jsou v tzv. sféře molekulového působení.Ad 2. Zcela jiná situace nastane, pokud je molekula kapaliny vzdálena od povrchu
méně než r0. Pak říkáme, že molekula je na povrchu kapaliny. Všechny tyto molekuly vytvářejí povrchovou vrstvu kapaliny. Působení přitažlivých sil není rovnoměrné. Existuje tudíž výslednice sil, která směřuje kolmo od povrchu kapaliny směrem do kapaliny. Její velikost se zmenšuje se zvětšující se vzdáleností od povrchu. Je-li vzdálenost větší než r0, tak molekula je uvnitř a výslednice je nulová. Povrchová vrstva tak působí na kapalinu molekulovým tlakem. Molekulový tlak působí v celém objemu, jeho hodnota je řádově pm » 109 Pa. To je hodnota tisíc krát větší, než je atmosférický tlak. Proto uvnitř kapaliny nejsou žádné volné prostory a kapaliny jsou málo stlačitelné.




